针对冠状病毒种类多、易突变、跨物种传播能力强等特点,找到其“变不了”的共同弱点,开发能防御多种冠状病毒的广谱药物,成为全球传染病防控的核心方向。
北京时间5月6日晚间,上海市重大传染病和生物安全研究院(以下简称“传研院”)青年研究员孙晓玉、复旦大学生物医学研究院研究员、传研院兼聘PI孙蕾、广州医科大学教授王延群、复旦大学基础医学院研究员、传研院兼聘PI谢幼华,于《自然》(Nature)杂志合作发表最新研究。

该研究首次解析了冠状病毒超广谱靶点S2’-helix的精细结构,揭开了奥密克戎在不改变靶点序列的前提下,实现抗体逃逸的全新机制,并提出“抗体小型化”通用应对策略,为下一代广谱抗冠状病毒药物研发奠定基础。
锁定“广谱命门”,筑牢研发根基
广谱药物研发的关键,在于找到病毒入侵关键蛋白(如刺突蛋白Spike)上的“广谱命门”。孙晓玉团队长期深耕呼吸道病毒感染机制及中和抗体研究,前期已在国际上率先鉴定出冠状病毒超广谱抗原表位Spike815-825(包含S2’切割位点),该表位在α、β、γ、δ四大冠状病毒属中均高度保守。同时,团队还筛选出靶向该表位的单克隆抗体76E1,可广谱中和已知的全部七种人类冠状病毒。这一超广谱靶点的发现,为广谱抗病毒药物研发筑牢了关键理论基石。
此外,孙蕾团队于2025年在《细胞》(Cell)杂志发表成果,首次解析了新冠病毒S蛋白处于“早期融合中间态”的构象结构。研究发现,原本隐藏在融合前Spike三聚体中的Spike815-825 表位,会在病毒入侵细胞、S蛋白构象转变为中间态时暴露出来。这一发现不仅验证了该表位的可及性,更为后续靶向该表位的药物及疫苗设计,提供了更精确的分子蓝图。

孙晓玉指导学生实验
靶点保守,为何抗体效力下降?目前,仍有一系列关键谜题未解。抗体如何与Spike815-825结合并阻断病毒入侵?令人困惑的是,研究团队发现了一个看似矛盾的现象:尽管该表位在包括奥密克戎在内的所有变异株中氨基酸序列依然高度保守,但靶向抗体对奥密克戎的中和效力却出现了不同程度的下降。病毒如何在不换“锁芯”的情况下,就让原本匹配的“钥匙”打了折扣?这些认知盲区成为该靶点走向应用的核心瓶颈。
抗体锁定入侵瞬间:S蛋白开放型早期中间态中的“S2’-helix真容”
团队经流式实验证实,新冠 S 蛋白结合 ACE2 受体后,会暴露 S2’-helix 并提升 76E1 抗体结合活性,提示该表位在 S 蛋白构象由融合前向融合后转变时瞬时出现。为了探究抗体究竟如何与Spike815-825结合并阻断病毒入侵,借助冷冻电镜技术,团队成功解析了76E1-Fab与新冠病毒野生型(WT)早期融合中间态S蛋白的复合物结构。该抗体通过结合Spike815-825,精准“锁定”病毒入侵时S蛋白的早期融合中间态结构。在此构象中,Spike815-825 包含S2’关键位点并呈现α-螺旋(helix)结构,研究团队将其命名为“S2’-helix”。
对比发现,未结合抗体的早期中间态S蛋白中,Spike815-825 为无规则loop结构,其空间位阻阻碍 76E1 结合;而当76E1 结合后,S1-ACE2 发生下移及外旋,在S2’-helix与S1-ACE2之间撑开足够大的空间使抗体嵌入,团队将这一独特构象定义为“开放型早期融合中间态”。
这一发现清晰揭示了76E1的中和机制:它如同分子锁靶向锁死病毒启动膜融合的关键部位—S2’切割位点,既与蛋白酶竞争结合、抑制 S2’位点切割及S蛋白构象变化,又通过空间占位物理性阻碍S 蛋白从中间态向融合后构象折叠,双重机制高效阻遏病毒感染。
奥密克戎逃逸新机制:不突变靶点,而是“隐藏”与“绕行”
值得注意的是,S2’-helix的关键抗原表位氨基酸,在包括奥密克戎在内的整个冠状病毒家族中均高度保守。但即便如此,奥密克戎突变株仍能对76E1、CoV44-62及C77G12等多款靶向该表位的抗体产生部分逃逸。功能实验揭示了一个有趣现象,将全长抗体(~150 kDa)“瘦身”为较小的Fab片段(~50 kDa),乃至更袖珍的单链抗体scFv(~27 kDa)后,这些小体型抗体对奥密克戎的结合与中和效力显著提升。这一现象强烈暗示,奥密克戎通过微调自身蛋白构象,为抗体结合设置了“物理屏障”。

孙晓玉(前排左一)、孙蕾(前排右一)团队合影
为进一步验证这一“空间位阻增强”机制,团队解析了76E1-Fab与XBB.1.5变异株早期融合中间态S蛋白的复合物结构,并与野生型进行对比分析。结果发现,当76E1结合时,XBB.1.5的S2’-helix发生一定位移,且其S1-ACE2“下沉”幅度更大。这意味着,在S2’-helix与S1-ACE2之间的空间要继续张大才可以嵌入抗体。抗体若要结合该靶点,需克服更大的空间阻力和更高的能量壁垒。因此,奥密克戎在S2’-helix靶点处制造“空间位阻增强”,是导致抗体逃逸的直接原因。
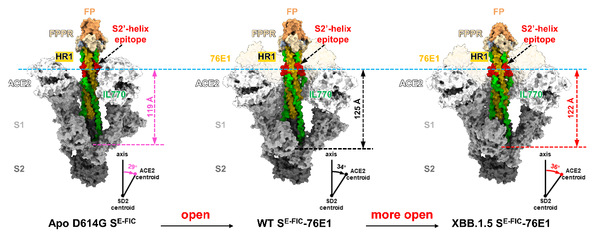
S2’-helix处的空间位阻效应影响抗体结合
研究还发现了第二条协同逃逸路径——“入侵途径转变”。已知奥密克戎会降低对细胞表面蛋白酶TMPRSS2的依赖,转而增强对组织蛋白酶CTSL介导的内吞体进入途径的利用,但这种改变的深层原因及对抗体药效的影响,长期以来始终不明。
研究发现,相较野生型毒株,TMPRSS2对奥密克戎S2’的切割活性显著降低,而CTSL对野生型和奥密克戎S2’均可高效切割,这可能正是奥密克戎主动改变入侵途径的原因。由于奥密克戎S2’-helix处对全长76E1抗体存在显著空间位阻,而CTSL切割活性不受影响,这提示76E1全长抗体抑制CTSL切割S2’的效果可能变差。实验进一步证实,76E1全长抗体能有效抑制 TMPRSS2 对野生型和奥密克戎 S2’的切割,但对 CTSL 切割奥密克戎 S2’的抑制效果却大打折扣。因此,奥密克戎通过强化对抗体抑制力较弱的内吞体进入路径,巧妙实现了二次逃逸。
研究最终锁定,S蛋白上的H655Y突变是驱动上述双重逃逸表型的核心。该突变可远程调控蛋白整体构象,一方面加剧S2’-helix靶点处的空间位阻,另一方面也能驱动病毒偏向内吞体入侵途径,从双重维度助力奥密克戎实现免疫逃逸。
普适性应对策略:“抗体小型化”强力逆转逃逸
奥密克戎双重逃逸机制的明晰,也指向了直接的破解策略。既然奥密克戎用“狭小空间”阻挡全长抗体,又“绕行”至抗体效力不佳的入侵路径,那就将抗体“小型化”,即可同时击破这两种逃逸机制。研究表明,“抗体小型化”策略效果显著:小型化的scFv抗体体积小巧,可灵活穿越靶点外围的空间屏障,高效对接靶点;同时,在CTSL主导入侵的细胞模型中,小型化抗体也能展现出强大的病毒中和能力。针对BA.5、XBB.1.5、EG.5.1、JN.1等一系列奥密克戎真病毒,以及SARS-CoV-1、HCoV-229E等其他人类冠状病毒,76E1-scFv均表现出远超其全长抗体的中和实力,充分证明了该策略的高效性与广谱性。
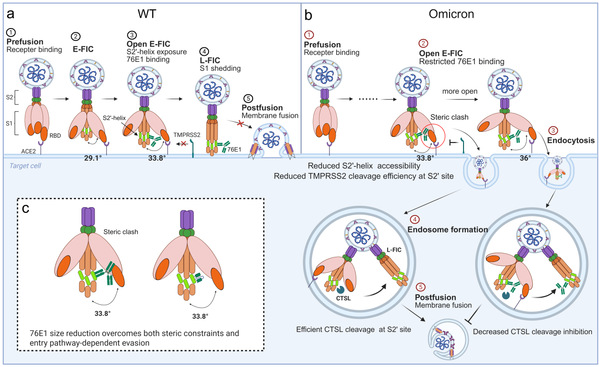
S2'-helix抗体中和与奥密克戎逃逸机制模式图
综上所述,研究利用中和抗体“锁定”新冠spike蛋白动态中间态,在病毒入侵瞬间揭开了超广谱靶点S2’-helix的真面目;系统阐明了奥密克戎通过“构象空间位阻”与“入侵途径转变”协同逃逸的分子机制,并在此基础上提出“抗体小型化”的高效通用策略。这些发现,为下一代超广谱抗病毒药物(如小分子抑制剂、纳米抗体等)的研发提供了重要的理论基础与设计指南。
传研院青年研究员孙晓玉,复旦大学生物医学研究院研究员、传研院兼聘PI孙蕾,广州医科大学教授王延群,复旦大学基础医学院研究员、传研院兼聘PI谢幼华为本论文的共同通讯作者,传研院博士生包智恒、复旦大学生物医学研究院博士生刘治民、广州医科大学博士后张昭勇为本论文的共同第一作者。研究得到复旦大学生物医学研究院研究员陈振国、传研院研究员黄忠及广州海关技术中心副主任医师张璐的帮助和支持。研究得到上海市市级科技重大专项、国家重点研发计划、国家自然科学基金等项目的资金支持。
原文链接:https://www.nature.com/articles/s41586-026-10462-2